
座談会:マルチフィールドから視る中性脂肪リスク ~SPPARMαの可能性~
山下:スタチンを用いたLDL-C低下療法による心血管イベントリスクの低下は約30%に留まっており1)、残りの約70%に含まれる個々のリスクを適切に評価し、介入していくことが重要です。その一つとして中性脂肪(TG:トリグリセライド)が挙げられます。高TG血症では小腸由来のカイロミクロンや肝臓由来のVLDLといったTGリッチなリポ蛋白が血中に多く存在し、これらの中間代謝産物であるレムナントや最終代謝産物であるsmalldenseLDL(sd-LDL)が動脈硬化を進展させると考えられています。本日はTGリスクについて、公衆衛生学、疫学・医療ビッグデータ、遺伝学・臨床研究等の様々な観点から討論したいと思います。
公衆衛生学から視るTGリスク
山下:はじめに岡村先生より、公衆衛生学の立場からTG管理の重要性について解説いただきます。
岡村:2001年に発表された国内のコホート研究では、非空腹時TG167mg/dL以上の群における冠動脈疾患発症リスクは84mg/dL未満の群の2.86倍であることが示され2)、TGリスクが注目される端緒となりました。その後の報告としてCIRCSでは空腹時と非空腹時に分けたリスク評価が行われ、空腹時ならびに非空腹時のいずれにおいてもTG増加に伴う虚血性心疾患リスクの上昇が認められています3)。
高TG血症の背景は多様であるため、そのリスクを正確に評価するためには、non-HDL-Cも同時に検討する必要があると考えられます。我々は吹田研究において、TGのカットオフ値を150mg/dL、non-HDL-Cのカットオフ値を190mg/dLとして心筋梗塞の発症リスクを検討しました。その結果、高TGかつ高non-HDL-Cの群で心筋梗塞発症リスクが最も上昇していました4)。
曽根:高TG血症による動脈硬化進展の原因にはsmalldenseLDL-C(sd-LDL-C)が関与していますが、公衆衛生学ではどのような報告があるのでしょうか。
岡村:吹田研究においてLDL-Cおよびsd-LDL-Cと各イベントリスクとの関係を検討したところ、いずれのイベントに関してもsd-LDL-CはLDL-Cよりもイベント予測能が高いことが示されました(図1)5)。このことは、sd-LDL-Cの背景にあるTG管理の重要性を示唆する結果と言えます。

疫学・医療ビッグデータから視るTGリスク
山下:続いて曽根先生より、疫学の立場からTG管理の 重要性について解説いただきます。
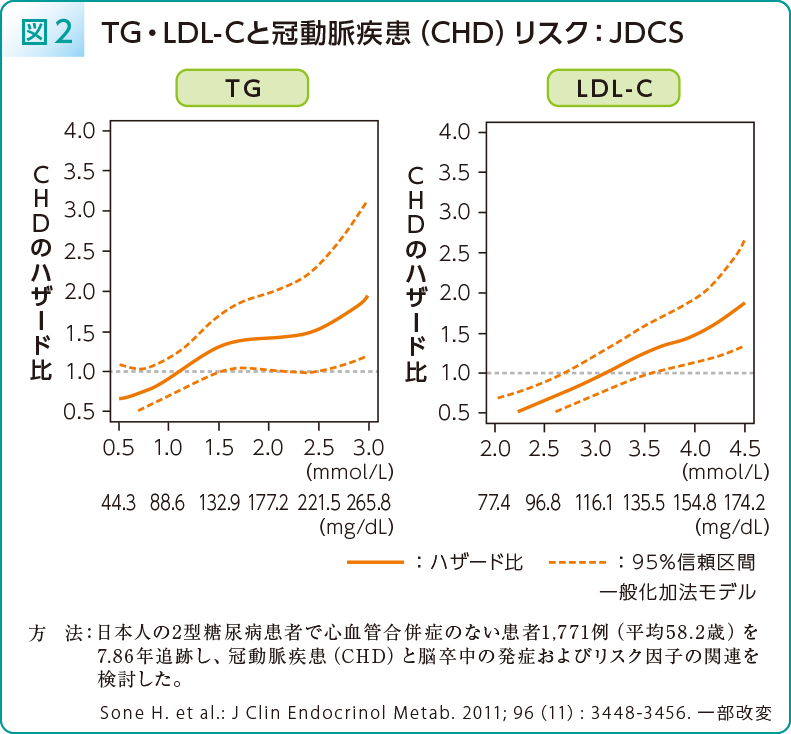
曽根:メタボリックシンドロームや2型糖尿病を伴う場合、インスリン作用不足によるリポ蛋白リパーゼ(LPL)の活性低下やホルモン感受性リパーゼの活性化に伴い、高TG血症や低HDL-C血症を示しやすくなります。日本人2型糖尿病患者を対象に我々が実施したJDCSでは、TG高値はLDL-C高値と同様に冠動脈疾患リスクを有意に上昇させることを示しました6)。また、TGとLDL-Cがともに高値であると冠動脈疾患リスクが相加的に上昇することや、LDL-Cと同様にTGも冠動脈疾患のハザード比とリニアな相関関係を示すことを報告しています(図2)6)。
山下:医療ビッグデータにおいてもTGと動脈硬化に関連する報告はあるのでしょうか。
曽根:レセプトデータベースより日本人男性をメタボリックシンドローム構成因子(高血圧、高TG血症、低HDL-C血症)の有無、肥満・糖尿病の有無で層別し、冠動脈疾患発症との関係について検討しています。その結果、肥満や糖尿病に加えてメタボリックシンドローム構成因子が一つ以上存在すると、冠動脈疾患発症リスクが上昇することが示されました7)。そのため、肥満や糖尿病に附随する高TG血症や低HDL-C血症、高血圧といったリスク因子を管理していくことが重要と考えます。
遺伝学・臨床研究から視るTGリスク
山下:続いて多田先生、TG管理の重要性について、遺伝学の立場から解説をお願いします。
多田:近年、ゲノムワイド関連解析が広く行われ、動脈硬化性疾患とTG関連遺伝子変異との関連が改めて明確となったことに加えて、メンデルランダム化解析の考案により、観察研究においても無作為化介入研究のように交絡因子を除外して因果関係を明らかにすることが可能になりました。この手法を用いて、TGに影響を及ぼすSNPはLDL-CやHDL-Cとは独立して冠動脈疾患と関連することが示されています8)。
岡村:TGに関わる遺伝子変異の報告として具体的にはどういうものがあるのでしょうか。
多田:TGに関連する遺伝子としてLPL、APOA5、APOC3、ANGPTL3等が挙げられます。これらの遺伝子変異によるTG低下と冠動脈疾患発症リスクの低下が関連することが示されています9)。
山下:TGと冠動脈疾患発症リスクとの関係について、最近の臨床試験ではどのような知見が得られているのでしょうか。
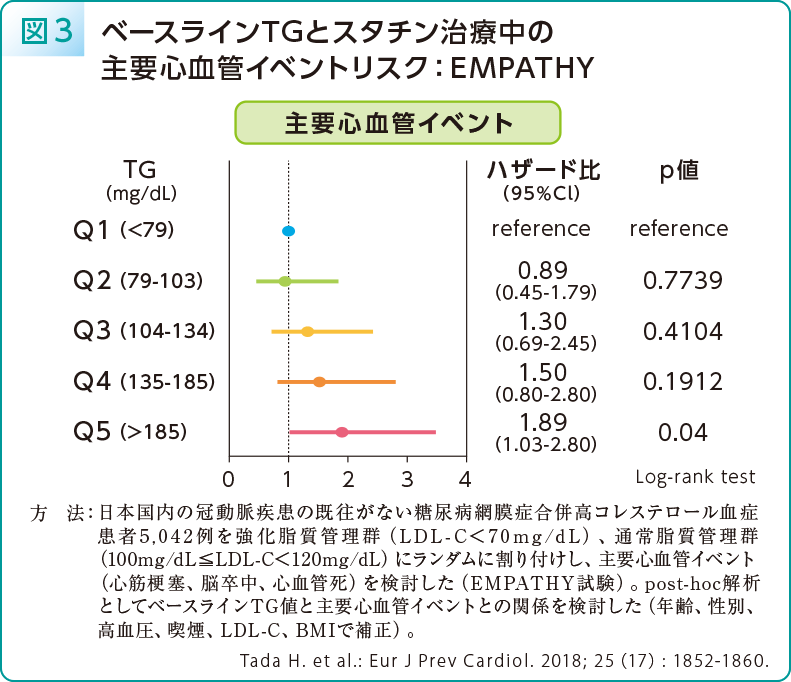
多田:海外臨床研究MIRACLのpost-hoc解析では、急性冠症候群においてスタチン治療下における空腹時TG高値は心血管イベント再発リスクを上昇させることが示されています10)。また、我々は多施設共同研究EMPATHYのpost-hoc解析を報告しており、日本人2型糖尿病患者においてもスタチン治療下におけるベースラインTG高値が主要心血管イベントリスクと関連していました(図3)11)。
SPPARMαペマフィブラートの有効性・安全性
山下:先生方のお話からTG管理の重要性が明らかになりましたが、高TG血症の新たな治療薬として「パルモディア®錠0.1mg」(一般名:ペマフィブラート)があります。ペマフィブラートは、PPARαを介した脂質代謝への効果を選択的に高め、その他の影響を少なくした選択的PPARαモジュレーター(SPPARMα:SelectivePPARαModulator)です12)。そのため『脂質異常症診療ガイド2018年版』では、ペマフィブラートはフィブラート系薬剤とは異なる「SPPARMα」のカテゴリーに位置づけられました。
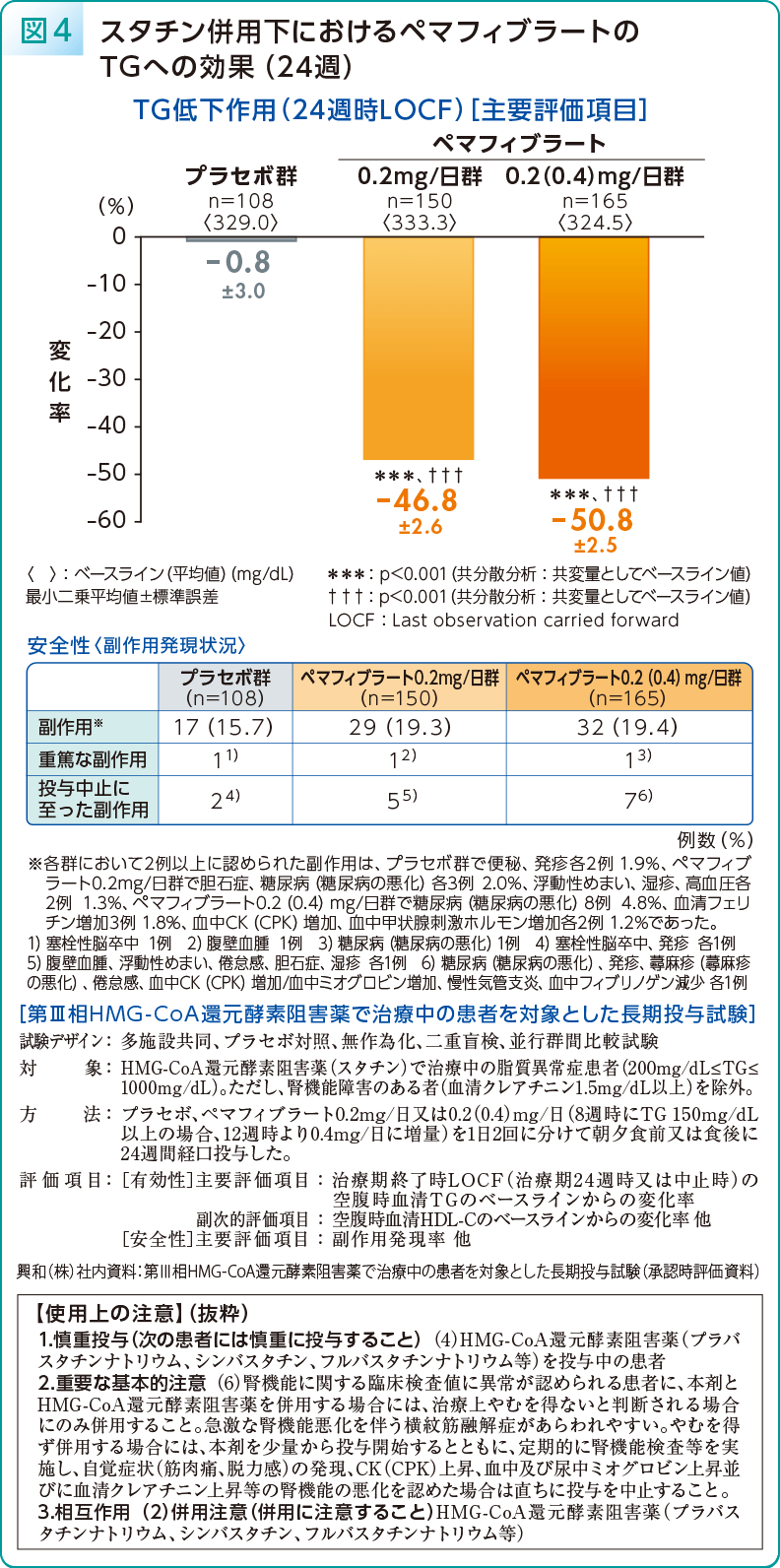
臨床的有用性については第II相用量探索的試験から、ペマフィブラートの優れたTG低下作用とHDL-C増加作用が確認されています13)。また第III相臨床試験において、スタチンへのペマフィブラート0.2mg/日追加投与によりTGが46.8%低下し(図4)、HDL-Cは17.8%増加することが示されています14)。本試験における副作用発現率はプラセボ群15.7%(108例中17例)、ペマフィブラート0.2mg/日群19.3%(150例中29例)でした。添付文書について2018年10月にSPPARMαおよびフィブラート系薬剤はスタチンとの併用に関する「原則禁忌」が解除され、これを「重要な基本的注意」に追記する形に使用上の注意が改訂されることになりました。しかしながら、横紋筋融解症リスクには十分注意した上で検討していただくことが重要です。
マルチフィールドから視るTG管理の重要性
山下:本日の内容を踏まえて、TGリスクとその管理について、先生方はどのようにお考えですか。
岡村:公衆衛生の分野では、これまでTGはLDL-CやHDL-Cの陰に隠れてあまり注目されてきませんでした。しかし、多方面からの研究成果がTG管理の重要性を示唆しており、保健指導等の場面でも重視すべきと考えられます。
曽根:レセプトデータベースを用いた検討が示唆するように、糖尿病や肥満だけに目を向けるのではなく、高血圧、高TG血症、低HDL-C血症といった個々のリスク因子を評価した上で、一つ一つ適切に介入していくことが重要だと思います。
多田:大規模臨床研究のpost-hoc解析から、スタチン投与下でもTG高値のリスクが示されたことは、臨床的に重要な知見だと考えています。
山下:ペマフィブラートは現在、2型糖尿病合併の高脂血症患者約10,000例を対象としたPROMINENT試験が進行中です15)。TG介入の意義に関する新たな知見が得られることに期待しています。本日はありがとうございました。
引用文献
1) Lim S. et al.: Int J Cardiol. 2013; 166(1): 8-14.
2) Iso H. et al.: Am J Epidemiol. 2001; 153(5): 490-499.
3) Iso H. et al.: Atherosclerosis. 2014; 237(1): 361-368.
4) Okamura T. et al.: Atherosclerosis. 2010; 209(1): 290-294.
5) Arai H. et al.: J Atheroscler Thromb. 2013; 20(2): 195-203.
6) Sone H. et al.: J Clin Endocrinol Metab. 2011; 96(11): 3448-3456.
7) Fujihara K. et al.: Diabetes Metab. 2017; 43(6): 543-546.
8) Do R. et al.: Nat Genet. 2013; 45(11): 1345-1352.
9) Tada H. et al.: Clin Chim Acta. 2019; 490: 1-5.
10) Schwartz GG. et al.: J Am Coll Cardiol. 2015; 65(21): 2267-2275.
11) Tada H. et al.: Eur J Prev Cardiol. 2018; 25(17): 1852-1860.
12) Fruchart JC.: Cardiovasc Diabetol. 2013; 12: 82.
13) 興和(株)社内資料:第II相用量探索的試験(承認時評価資料)
14) 興和(株)社内資料:第III相HMG-CoA還元酵素阻害薬で治療中の患者を対象とした長期投与試験(承認時評価資料)
15) Pradhan AD. et al.: Am Heart J. 2018; 206: 80-93.

